CAR-T VS BsAb:由ASH年會臨床數(shù)據(jù)比較兩種療法,孰強孰弱,?
CAR-T療法治療血液腫瘤的獨特優(yōu)勢使其再次成為ASH年會的熱點,而與其作用機理類似的雙特異性抗體也不甘示弱。ASH年會上Regeneron和Amgen相繼公布其雙特異性抗體優(yōu)異的早期臨床數(shù)據(jù),療效可媲美CAR-T療法,,與此同時Bluebird、Celgene,、Juno,、Allogene和南京傳奇也公布了其CAR-T療法的早期臨床數(shù)據(jù),孰強孰弱,,筆者在文中簡要比較了兩種療法,。
? CAR-T與BsAb
嵌合抗原受體T細胞療法(Chimeric Antigen Receptor T-Cell Immunotherapy,,CAR-T),,與雙特異性抗體(Bispecific Antibody,BsAb)療法具有類似的作用機制,,兩者均可以使T細胞有效地靶向腫瘤相關(guān)抗原,,增強T細胞對腫瘤細胞的殺傷作用。
CAR-T療法在體外對患者T細胞進行基因改造,,即將識別腫瘤相關(guān)抗原的單鏈抗體(scFv),、跨膜的共刺激結(jié)構(gòu)域(如CD28或CD4-1BB)和T細胞的活化基序(如CD3ζ或FcεRIγ)結(jié)合為一體,通過基因轉(zhuǎn)導(dǎo)方法轉(zhuǎn)染T細胞形成CAR-T細胞,,并在體外擴增后回輸?shù)交颊唧w內(nèi)發(fā)揮作用,。CAR-T細胞可通過表達單鏈抗體以增強結(jié)合腫瘤細胞的能力,從而增加對癌細胞的殺傷,。
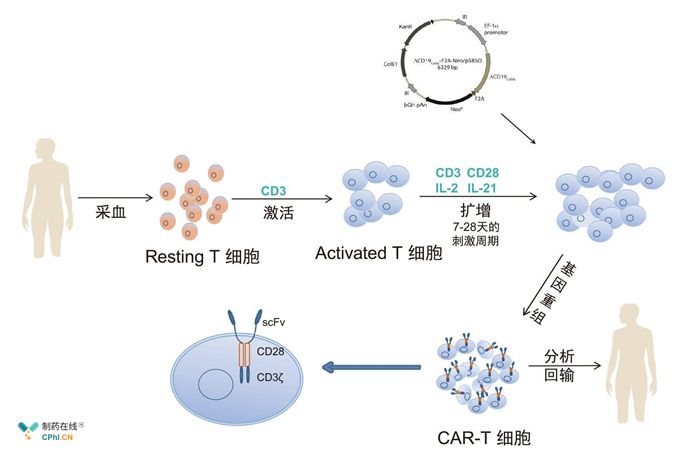
CAR-T療法(圖片來源于網(wǎng)絡(luò))
雙特異性抗體(Bispeific Antibody,,BsAb)按結(jié)構(gòu)區(qū)分主要有兩大類:含F(xiàn)c區(qū)的BsAb(IgG-like)與不含F(xiàn)c區(qū)的BsAb(Non-IgG-like),其Fab區(qū)域的兩條單鏈抗體(scFv)可以分別與T細胞抗原(如CD3等)和腫瘤細胞抗原(如EpCAM等)結(jié)合,,將T細胞與腫瘤細胞鏈接在一起,,啟動T細胞對腫瘤的精準殺傷。BsAb的制備方法有:化學(xué)偶聯(lián)法,、雙雜交瘤融合法(Konb-in-hole等)和基因工程,。
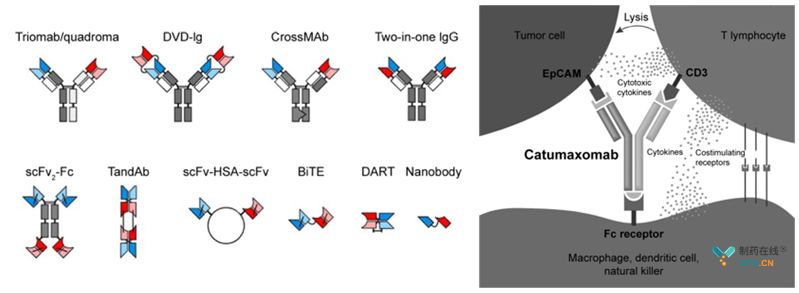
BsAb結(jié)構(gòu)(左)及作用機理(右)(圖片來源于參考1)
? FDA批準的CAR-T療法和BsAb
2017年,F(xiàn)DA相繼批準兩款治療血液瘤的CAR-T療法:Kymriah和Yescarta,;2014年,,首款BsAb Blincyto獲得FDA批準,用于治療復(fù)發(fā)性/難治性前體B細胞急性淋巴細胞白血??;2017年,F(xiàn)DA又批準了Roche研發(fā)的治療A型血友病的BsAb Hemlibra,,其分別靶向凝血因子IXa和X,。
另外,,2009年Trion制藥公司研發(fā)的Catumaxomab在歐盟獲得批準上市,是全球首款獲批的BsAb,。Catumaxomab是一種抗CD3和上皮細胞粘附分子(EPCAM)的小鼠雙特異性抗體,,用于治療EPCAM陽性腫瘤的惡性腹水患者。
此外還有許多正處于臨床試驗階段的CAR-T療法和BsAb項目,,CAR-T療法:LCAR-B38M,、bb2121、CART-BCMA,、JCARH125,、FCARH143、bb21217等,;BsAb:AMG330,、AMG420、REGN1979,、Mosunetuzumab,、COVA322、Remtolumab,、RG6026等,。
表1 FDA批準的CAR-T療法和BsAb

? ASH年會上公布的抗BCMA CAR-T療法和BsAb的臨床數(shù)據(jù)
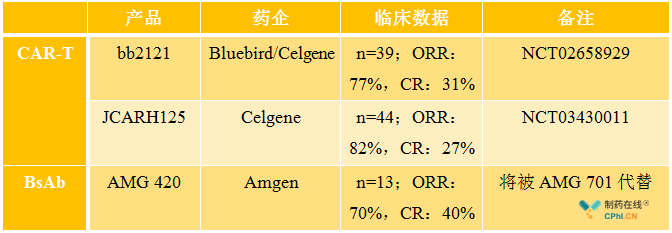
2018 ASH年會上,Amgen再次展現(xiàn)了其雙特異性T細胞結(jié)合器(BiTE)AMG420治療復(fù)發(fā)/難治性多發(fā)性骨髓瘤(MM)的臨床數(shù)據(jù),,AMG420的靶點為分別靶向BCMA和CD33,。在劑量遞增(0.2-800 ug/天)的臨床I期研究中,13名MM患者接受400 ug/天劑量的AMG420治療,,達到70%(7/10)的客觀緩解率(ORR)和40%的完全緩解率(CR,,即4名患者微小殘留病灶檢測為陰性),其中6名患者的緩解期已經(jīng)達到7.5個月,。
然而與同類抗BCMA的CAR-T療法相比,,AMG420在療效上要稍遜一些。bb2121,,Bluebird和Celgene共同研發(fā)的靶向BCMA的CAR-T療法,,在12名患者中的ORR達到83%;Celgene和Juno開發(fā)的同樣靶向抗原BCMA的JCARH125也取得了82%(36/44)的客觀緩解率,。
表2 ASH年會上靶向BCMA治療MM的CAR-T療法和BsAb的臨床試驗
就安全性數(shù)據(jù)來講,,CAR-T療法的主要副作用為細胞因子釋放綜合征(CRS)和神經(jīng)毒素,ASH年會上有學(xué)者將靶向BTK抑制劑Ibrutinib和CAR-T療法聯(lián)合用藥,,有效的降低了CAR-T療法的副作用,,另外合理的臨床治療方案也可以降低CAR-T療法的副作用。
而對于BsAb,安全性還是主要的考量,,在AMG420的臨床試驗中出現(xiàn)兩名患者死亡事件,,雖然Amgen表明與患者接受AMG420治療無關(guān)。在此之前,,曾有兩項BsAb候選新藥COVA322(Phase I:NCT02243787)和4G7 × H22(Phase I:NCT00014560)分別因為安全性和毒性而終止開發(fā),。
另外由于BsAb的特殊結(jié)構(gòu),如AMG420(BiTE)等,,其一般具有較短的半衰期,,為保證療效需要持續(xù)不斷的注射,這對患者來講也是一種負擔,。就AMG420半衰期短的劣勢,,Amgen已經(jīng)著手開發(fā)下一代、半衰期更長的BiTE--AMG701,,以便獲得相對于CAR-T療法的競爭優(yōu)勢,。
表3 CAR-T療法和BsAb的優(yōu)缺點比較

參考來源:
1. Bispecific antibodies: design, therapy, perspectives;
2. At ASH, bispecific cancer therapies make a mark,;
3. Bispecifics vs CAR-T: Analysts select the big winners - and losers - at #ASH18's biggest ever datapalooza,。
